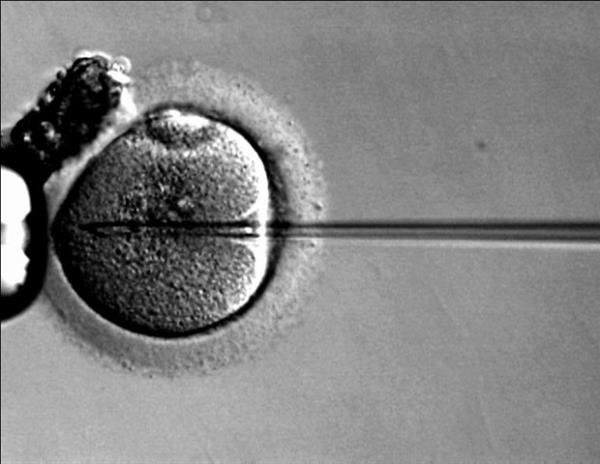
来自的里雅斯特国际高等研究学院(SISSA)的一个研究小组通过将基因疗法应用于胶质母细胞瘤获得了非常有希望的结果。在小鼠身上进行的体外和体内试验提供了非常明确的结果,模型表明,这种治疗至少针对肿瘤代谢的六个不同点。基因疗法是一种选择性攻击肿瘤的技术,它可能为对抗这种致命的癌症带来希望。对于这种癌症,手术几乎是不可能的,化疗和放疗对非常严重的复发无效。这项研究发表在Oncotarget杂志上。
就在几天前,新闻界(特别是英语国家的新闻界)热情地宣布了一项研究的发表,该研究非常详细地描述了乳腺癌的遗传学,许多人认为这一发现标志着与这种癌症的斗争取得了突破。这类消息证实了这样一种印象:在不久的将来,与癌症的战争将在遗传学的战场上进行。意大利也在这方面努力。例如,在SISSA, Antonello Mallamaci和他的团队刚刚发表了应用基因疗法治疗胶质母细胞瘤的非常有希望的结果,胶质母细胞瘤是脑肿瘤中最常见和最具攻击性的一类。胶质母细胞瘤的诊断实际上等于即将被判死刑:“手术很少能治愈,因为这些肿瘤会在健康组织中逐渐扩散,而且化疗和放疗也几乎没有效果。”在很短的时间内,非常激烈的循环发展,这标志着结束,”安东内洛·马拉马奇解释说,他是SISSA教授,也与Telethon基金会合作。“我们的方法是完全不同的:我们将一个给定基因的额外拷贝引入肿瘤细胞,从而削弱它们的生殖能力,导致它们自杀。”
Mallamaci并不是肿瘤学家,他是在对一种叫做Emx2的特殊基因进行了多年的深入研究后产生了这项研究的想法。这位科学家解释说,这种基因的特征之一是在胚胎生长过程中抑制星形胶质细胞的增殖。胶质细胞,包括星形胶质细胞,是神经系统的一部分,在那里它们滋养和保护神经元,并精细地调节它们的功能。
“我们知道,在神经系统发育的早期阶段,只有神经元生长,而神经胶质细胞只有在神经元生长几乎完成时才开始增殖,”SISSA研究科学家、该论文的第一作者卡门·法尔科内解释说。“在我们之前的研究中,我们发现Emx2在神经元生成阶段的表达水平非常高,而当神经胶质细胞开始生长时,它的作用急剧下降。所以这个基因在一定程度上控制星形胶质细胞的生长。”
如果它可以阻断星形胶质细胞,为什么不尝试用它来阻断胶质母细胞瘤呢?“这些肿瘤与星形胶质细胞有许多共同的特征,”Mallamaci评论道,“因此我们有了利用它们的想法。”由于IST在热那亚的贡献,它为我们提供了各种胶质母细胞瘤的培养物,我们开始做一些体外测试。”法尔科内和马拉马奇解释说,这些测试“超出了我们最乐观的预期”:“在几乎所有的样本中,肿瘤组织在不到一周的时间里就崩溃了。”
在这一点上,研究继续向两个方向发展。该团队首先在体外模拟了治疗基因“开启”和最终效果之间的分子机制,发现该基因在不少于6个点上攻击肿瘤代谢,研究人员将这一结果定义为“非常稳健”。
体外实验结束后,研究小组在小鼠身上开始了第一次体内实验,并采取了一切必要的预防措施,以防止动物遭受不可接受的痛苦。“因此,为了防止对健康细胞、神经元和星形胶质细胞的损害,我们选择了一种特殊的‘启动子’,这是一段DNA,它只会在肿瘤细胞中激活治疗基因,而不会攻击其他细胞,我们复制了与第一次体外试验相同的结果。”
基因治疗的基础是将特定基因插入宿主细胞的基因组中,这样这些基因就可以通过借用宿主细胞的遗传机制在细胞内发挥作用。一点遗传密码是如何添加到活细胞中的?科学家使用病毒自然采用的机制。病毒是一种奇怪的实体:虽然它们有自己的基因组,但它们不能自己复制和繁殖。出于这个原因,它们潜入细胞,将自己的DNA插入宿主基因组,这样细胞就开始为它们工作,复制它们的基因,形成其他病毒。法尔科内解释说:“通过使病毒无害,也就是说,通过清空包含其基因组的外壳,并用治疗性基因填充它,我们可以向宿主细胞添加新的基因,或内源性基因的增强版本。”
这正是Mallamaci和同事们所做的:他们将一种特别活跃的Emx2引入肿瘤细胞。到目前为止,结果是明确的,并且已经证明Emx2能够杀死至少四种不同类型的胶质母细胞瘤细胞,无论是在体外还是在啮齿动物体内,都不会损害神经系统的健康细胞。由于他们还观察到治疗针对肿瘤过程的许多点,因此有很好的机会有效地对比侵袭性复发的发展。“为了形成这些,必须有一个选择最强肿瘤细胞的过程。通过在不同的点上瞄准他们,我们提高了选择过程的标准,希望我们能防止复发,”马拉马奇总结道。“现在我们计划将体内试验扩展到其他胶质母细胞瘤。通过大量的努力和一点运气,我们希望在几年的时间里,所有这些都能转化为对受这种疾病折磨的不幸患者的切实好处。”




