合成了氨基聚羧酸锌(II)与1,10-菲罗啉和2,2′-联吡啶基{[Zn(IDA)(H2O)2]、[Zn(IDA)(bipy)(H2O)]·2H2O和[Zn(IDA)(phen)(H2O)]·2H2O}配合物。为了确定合成的配合物的组成和纯度,采用元素分析。然后,研究了在CTAB和Triton X-100两种表面活性剂溶剂中,两个水分子在亚氨基二乙酸锌配合物中取代1,10-菲罗啉和2,2′-联吡啶的动力学。采用停流法进行了动力学研究。在288.15、293.15和298.15 K 3种不同温度下,配合物[Zn(IDA)(H2O)2]的摩尔浓度为1 mM;在配体(1,10-菲罗啉和2,2′-联吡啶)的摩尔浓度不变的情况下,0.75 mM、0.5 mM和0.25 mM为0.05 mM。在260 nm波长处测量了反应动力学运行过程中的吸光度变化。通过动力学研究,确定了反应的顺序,并利用Glint程序用停止流法确定了两个水分子取代n给体配体的反应速率的可观察速率常数。下一步,用电位滴定法测定了配合物{[Zn(IDA)(H2O)2]、[Zn(IDA)(bipy)(H2O)]·2H2O和[Zn(IDA)(phen)(H2O)]·2H2O}在水溶液中的热力学参数。Hyperquad2018程序用于确定稳定性常数。此外,用电导滴定法测定了锌(II)与n -杂环配体在水溶液中的配合物的化学计量。
复杂的化合物表现出许多不寻常的性质,并且有几个重要的原因。首先,许多工业催化剂是含有金属离子的配合物,如Grubbs催化剂在络合物中以钌(II/III)离子为中心原子,在烯烃复分解反应中具有较高的催化活性[1,2,3,4]。其次,过渡金属配合物在生物化学中是必不可少的,如含铁(II/III)离子[5,6]、铜(II)离子[7,8]和锌离子[9,10]的配合物是生物反应中某些酶或催化剂的关键组分。配位球中含锌离子的络合物值得特别注意。锌离子在许多金属酶中发挥重要作用,因为它们具有d10价电子构型,因此它们不受配体场的影响,这可能决定了所得到的配合物的几何形状[11,12,13,14]。锌在人体中起着重要的作用。它是许多酶的活性中心,例如碳酸酐酶。碳酸酐酶的作用使得这种酶每秒可以释放106分子一氧化碳(IV)[14,15,16,17]。这是最快的酶促反应之一。锌(II)的聚羧酸配位化合物是一类非常有趣的理化和生物学研究的化合物。它们被用于许多领域:医学、光子学、生物研究[18,19]。它们也被用作半导体[20]。以过渡金属为中心离子的聚羧酸盐配位化合物具有有趣的磁性、生物学和结构特性[21,22,23,24]。除了金属离子外,位于配合物配位球内的配体也值得关注。对螯合配体的主要兴趣源于它们形成稳定的复合物的能力。1,10-菲罗啉[25,26,27,28],2,2 ' -联吡啶基[29,30,31]是n -杂环螯合配体,可与锌、铜(II)或铁(III)离子形成稳定的配合物。1,10-菲罗啉以九种结构异构体的形式存在,这些异构体在化学键的排列和氮原子的位置上有所不同。反过来,2,2 ' -联吡啶可以以六种结构异构体的形式出现,不同的是氮原子的位置和化学键的排列。1,10-菲罗啉作为螯合配体也愿意形成配位关节,其中心离子也主要是离子:锌、铜(II)或铁(III)。在水基配体与n -杂环配体(1,10-邻菲罗啉或2,2′-联吡啶)的取代反应中,表面活性剂[32]即表面活性化合物作为溶剂,它们会影响所研究动力学反应的可观察速率常数的值[33,34]。这是由于表面活性剂可以模拟胶束和膜细胞之间的物理相互作用[35,36]。近年来,人们对复合物中一种配体与其他配体取代的动力学研究兴趣显著增加。首先,在复杂的化合物中,单位点配体被螯合配体取代,因为在配位球中含有螯合配体的复杂化合物比含有单位点配体的复杂化合物稳定得多。化学动力学的中心公理是相信每一个存在的化学反应都是共存的基本反应的结果,形成了一个平行和连续过程的网络[37,38,39]。停流法是研究快速化学反应的最佳方法之一。停流法使研究液相中相对快速的化学反应(半衰期在毫秒量级)的动力学成为可能。停止流动技术的优势主要在于使用小体积的溶液(这是经济的),并且测试在厌氧条件下和恒温下进行[40,41,42,43]。
本文描述了两个水分子n -杂环配体(1,10-菲罗啉和2,2′-联吡啶)在[Zn(IDA)(H2O)2]中的取代反应速率。以表面活性化合物CTAB和Triton X-100为反应介质进行动力学研究。测定了所测反应的速率常数。在得到试验结果的基础上,用图解法确定了反应顺序。采用电位滴定法(PT)和电导滴定法(CT)表征了化学物质在水溶液中的热力学稳定性。此外,还提出了所研究的取代反应的关联机理。
所有复杂化合物的合成都是根据文献[44]中描述的程序进行的。
锌(IDA) (H2O)2]n
称量3.19 g亚氨基二乙酸,放入50ml圆底烧瓶中,开始合成。将酸溶解在少量水中后,将烧瓶放在磁力搅拌器上加热到50℃。加热时,将2.54 g Na2CO3·10H2O缓慢加入烧瓶中。待二氧化碳完全析出后,将5.54 g ZnCl2·6H2O溶于水中,少量加入溶液。结晶产物[Zn(IDA)(H2O)2]n经减压过滤后干燥。
(锌(IDA)(苯酚的)(H2O)]·2 h2O
在圆底烧瓶中,3.19 g H2IDA溶于少量水中。将溶液置于磁力搅拌器上加热至50℃,分次加入2.54 g Na2CO3·10H2O。待CO2以气体形式完全蒸发后,将5.54 g ZnCl2·6H2O溶于水中制备的溶液从溶液中缓慢加入。在配合物的合成结束时,加入4.75 g 1,10-菲罗啉。用真空过滤装置对[Zn(IDA)(phen)(H2O)]·2H2O的析出晶体进行过滤。
(锌(IDA) (bipy) (H2O)]·2 h2O
将0.80 g H2IDA溶于圆底烧瓶中的小量水中。将溶液置于磁力搅拌器上,加热至50℃,分次加入0.64 g Na2CO3·10H2O。待CO2气泡停止释放后,再缓慢加入3.03 g Zn(NO3)2·6H2O和0.94 g 2,2′-联吡啶。然后在减压下过滤掉沉淀的络合物[Zn(IDA)(bipy)(H2O)]·2H2O,并使其干燥。
用Vario EL分析仪Cube对合成的锌(II)配合物进行元素分析。结果表明:[Zn(IDA)(H2O)2]n: C, 20.72%, H, 3.75%, n, 6.19%。分析的计算的。: c, 20.66%, h, 3.90%, n, 6.02%。(锌(IDA)(苯酚的)(H2O)]·2水:C, 45.01%, H, 3.84%, N, 8.98%。分析的计算的。: c, 44.62%, h, 4.44%, n, 9.76%。(锌(IDA) (bipy) (H2O)]·2水:C, 44.87%, H, 3.82%, N, 10.81%。分析的计算的。: c, 45.66%, h, 3.69%, n, 11.91%。
采用应用光物理公司的sx18 MV-R测定仪,采用分光光度停流法对反应动力学进行了测试。停流法测定反应动力学的条件为:恒温时间30min, CTAB和Triton X-100研究反应动力学的温度分别为288.15、293.15和298.15 K。监测反应过程中吸光度变化的波长:260 nm。测试反应的测量时间:0.2 s。对[Zn(IDA)(H2O)2]的浓度进行了反应动力学测量:1 mM;配体1,10-菲罗啉和2,2′-联吡啶的浓度为0.05 mM。
电位滴定使用CerkoLab微滴定系统,测量池配有磁力搅拌器、Schott-Blue Line 16 pH组合电极和Hamilton 5ml注射器。测量在298.15 K (Lauda E100循环恒温器)下进行。滴定溶液包含:(1)H2IDA (1.5 mM) + Zn2+ (1.5 mM), (2) H2IDA (1.5 mM) + Zn2+ (1.5 mM) + bipy (1.5 mM), (3) H2IDA (1.5 mM) + Zn2+ (1.5 mM) + phen (1.5 mM)。采用50mm标准NaOH溶液作为滴定剂。每60秒加入0.002 mL的NaOH溶液。电位测量中pH电极的校准按照IUPAC(国际纯粹与应用化学联合会)的要求进行。配制精确已知pH值的标准溶液(缓冲溶液)。确保参比电极(标准电位电极)充有适当的电解液。确保电极清洁,无任何杂物。在三个不同的pH点校准电位电极。在每个校准的标准溶液中测量电极的pH值。确保电极稳定,pH值读数可重复。校准和测量重复了几次,以确认结果的可重复性,并确保电极正确校准。
电导滴定在Cerko实验室设备上使用CD-201电导池(常数k=0.096 cm?1,HYDROMET),磁力搅拌器和5ml Hamilton注射器进行。电极的标准化使用Hamilton购买的氯化钾溶液进行,其电导率为84μS/cm溶液和200μS/cm溶液。电导率滴定在298.15 K下进行(Lauda E100循环恒温器)。滴定溶液包含:1)H2IDA (1mm) + Zn2+ (1mm), 2) H2IDA + Zn2+ (1mm) + bipy (1mm), 3) H2IDA + Zn2+ + phen (1mm)。50mm NaOH溶液作为滴定剂。NaOH溶液每30 s加入0.02 mL。
摘要
介绍
材料与方法
结果与讨论
结论
数据可用性
参考文献
致谢
作者信息
道德声明
搜索
导航
#####
采用停流法在CTAB(aq)和SDS(aq)两种表面活性溶剂下测试了反应动力学。首先,对底物(Zn(IDA)(图1)、bipy和phen)、体积比为1:1的Zn(IDA)与phen或bipy以及配合物Zn(IDA)(phen)和Zn(IDA)(bipy)(图1)的紫外光谱进行登记,以选择合适的波长进行动力学研究(图2)。
图1
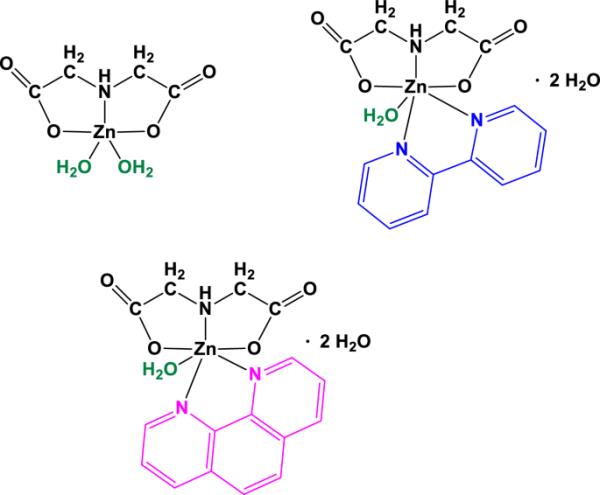
所测配合物[Zn(IDA)(H2O)2] (A)、[Zn(IDA)(bipy)(H2O)]·2H2O (B)和[Zn(IDA)(phen)(H2O)]·2H2O (C)的分子式
图2
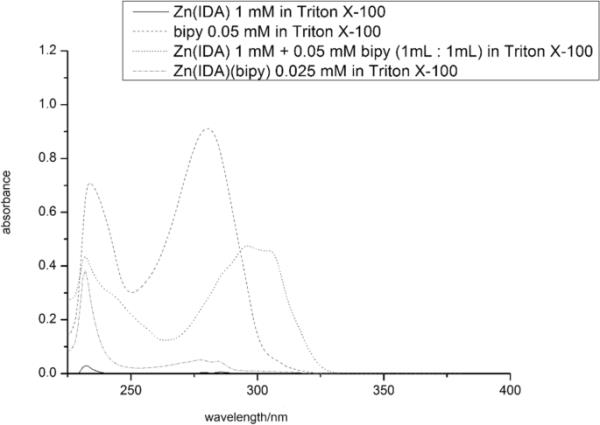
1 mM [Zn(IDA)(H2O)2]、0.05 mM bipy、0.025 mM [Zn(IDA)(H2O) (H2O))(H2O)]和1 mM [Zn(IDA)(H2O)2]与0.05 mM bipy按1:1体积比的混合物在0.4 mM Trition X-100水溶液中的紫外光谱
在CTAB和Triton X-100中,两个水配体在锌配位球中被2,2 ' -联吡啶或1,10-邻菲罗啉分子取代。用图解法确定了反应顺序。吸收变化随时间的线性调整证实了所研究的反应是伪一级反应。可观测速率常数(kobs)的值使用非线性最小二乘法拟合伪一级反应动力学的未变换原始方程(图3)。这意味着其中一种底物已被用于大量过量(图4、5、6、7)。
图3
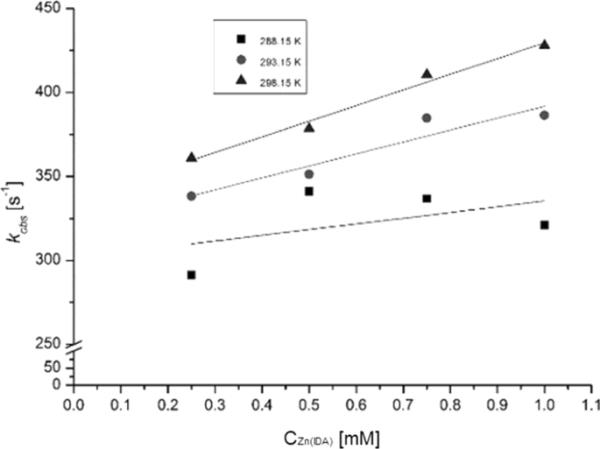
在Triton X-100水溶液中,特定温度下[Zn(IDA)(H2O)2]与bipy反应的kobs=f (CZn(IDA))曲线
图4
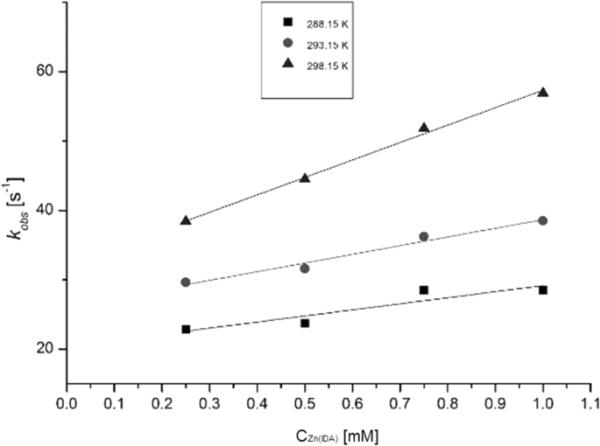
在Triton X-100水溶液中,特定温度下[Zn(IDA)(H2O)2]与苯的反应的kobs=f (CZn(IDA))曲线
图5
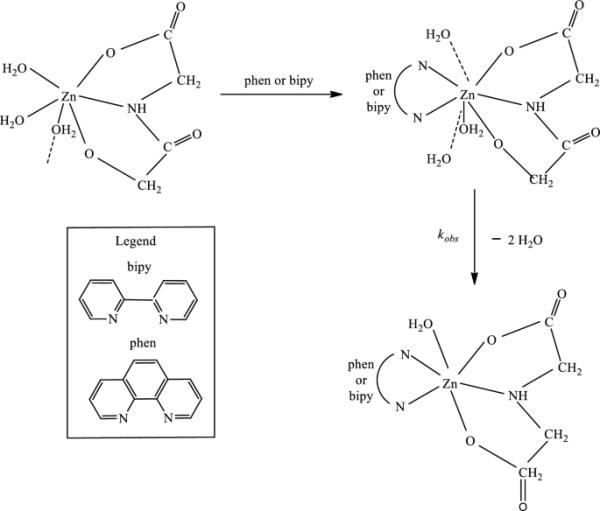
在CTAB水溶液中,[Zn(IDA)(H2O)2]在规定温度下与bipy反应的kobs=f (CZn(IDA))曲线
图6
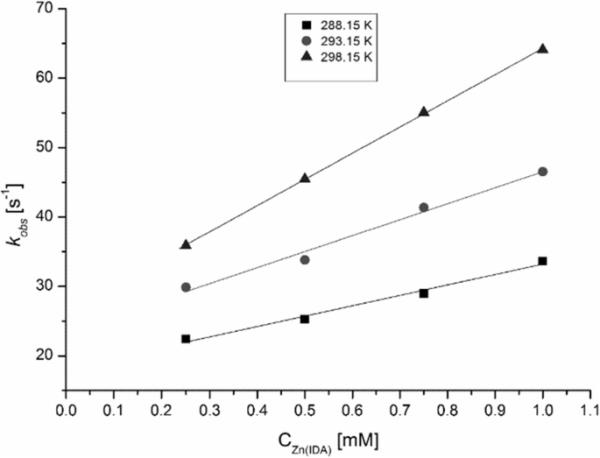
[Zn(IDA)(H2O)2]与苯在CTAB水溶液中特定温度下的反应的kobs=f (CZn(IDA))曲线
图7
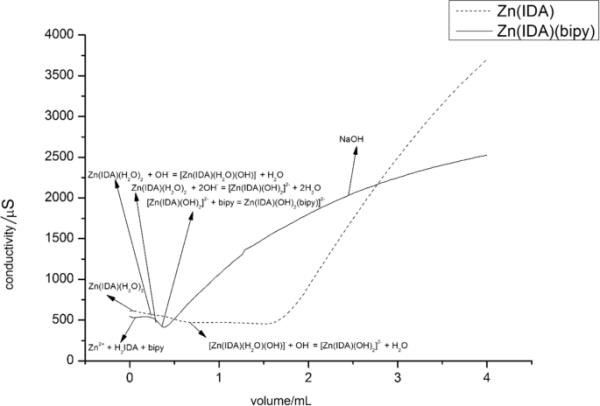
锌离子与亚氨基二乙酸、1,10-菲罗啉和2,2′-联吡啶的电导率滴定曲线
通过对所得结果的分析,可观察到的速率常数kobs随[Zn(IDA)(H2O)2]浓度和温度的升高而增大。这种关系与活性配合物的理论是一致的。二元配合物与双酚配体的反应比锌(IDA)与苯的反应快得多。在CTAB水溶液中,与bipy的反应速度比与phen的反应快5倍(基于298.15 K时[Zn(IDA)(H2O)2]=1 mM浓度的kobs值的比较)。
根据得到的测试结果,发现配合物[Zn(IDA)(H2O)2]n与1,10-菲罗啉和2,2′-联吡啶的反应为一级反应。方案1显示了在配合物[Zn(IDA)(H2O)2] N中,两个水分子取代N,N ' -杂环双齿氮配体(phen或bipy)的反应机理。所提出的机制是基于联想机制的假设。结合取代机制遵循金属配合物中配体取代的共同途径。在第一步中,bipy或phen配体通过来自配体的两个氮原子附着在复合物上。此时形成中间体,其配位数比底物的配位数大1。下一阶段,一个水分子被分离,形成稳定的配位化合物:[Zn(IDA)(phen)(H2O)]和[Zn(IDA)(bipy)(H2O)]。
方案1

提出了[Zn(IDA)(H2O)2]n配合物与1,10-菲罗啉或2,2′-联吡啶在水溶液中取代反应的机理
为了确定配合物[Zn(IDA)(H2O)2]、[Zn(IDA)(phen)]和[Zn(IDA)(bipy)]在水溶液中的热力学稳定性,采用了电位滴定法。为了确定决定被测系统在水溶液中稳定性的热力学参数,使用了Hyperquad2018程序。理论模型的应用使实验数据与理论数据相关联。为了确定水溶液中的恒定平衡,使用了以下模型:
式中:p, q, r, s为反应的化学计量系数,M=Zn2+, L=亚氨基二乙酸阴离子,r=bipy或phen, H=质子(表1,2,3)。
表1 logβpqrs矩形锌(IDA)复合物的值(括号中的标准差)
表2 logβpqrs矩形Zn(IDA)(bipy)复合物的值(括号中的标准差)
表3 logβpqrs矩形Zn(IDA)(phen)复合物的值(括号中的标准偏差)
用电位滴定法测定了[Zn(IDA)(H2O)2]、[Zn(IDA)(phen)]和[Zn(IDA)(bipy)]及其衍生物在水溶液中的热力学稳定性。在ML形式中,与由[Zn(IDA)(phen)] (logβ1100=9.99)和[Zn(IDA)(H2O)2] (logβ1100=7.88)衍生的形式相比,由化合物Zn(IDA)(bipy) (logβ1100=10.37)衍生的形式在水溶液中具有最大的稳定性。与其它亚氨基二乙酸多羧基化合物(logβ1100 [Co(IDA)(H2O)2]=8.54[45])的累积稳定性比较,锌(II)化合物[Zn(IDA)(H2O)2]在水溶液中表现出最高的热力学稳定性。此外,在水溶液中,在[Zn(IDA)(H2O)2]中以ML2 (logβ1200=14.44)的形式表现出最大的稳定性,在Zn2+-IDA-phen体系中以MLR (logβ1110=12.85)的形式表现出最大的稳定性,在Zn2+-IDA-bipy体系中以MLR (logβ1110=13.92)的形式表现出最大的稳定性。
在附图中,可以观察到两条滴定曲线。蓝色曲线表示[Zn(IDA)(H2O)2]的电导滴定。在电导率611 ~ 600 μS范围内,这种形态出现在曲线的开始。在600 ~ 469 μS范围内电导率下降,形成[Zn(IDA)(H2O)(OH)]?。在下一步中,形成[Zn(IDA)(OH)2]2?,电导率的变化几乎难以察觉,变化范围在469 ~ 452 μS之间。第二条曲线为滴定体系Zn2+ + H2IDA + bipy。在第一阶段,可以观察到溶液的电导率从528 μS略微增加到570 μS。然后观察到溶液电导率急剧下降(570 ~ 411 μS),形成[Zn(IDA)(OH)2]2?。最后一步生成[Zn(IDA)(OH)2(bipy)]2?,并在432 μS下观察到电导率的快速增加。这是由于NaOH的加入产生了过量的OH离子。
通过分析表面活性剂水溶液中锌(II)和铜(II)亚氨基二乙酸配合物取代反应速率研究的动力学数据可以看出,涉及2,2′-联吡啶的取代反应比涉及1,10-菲罗啉的取代反应发生得更快(图8,9)。在CTAB和Triton X-100水溶液中的停流动力学研究中都发现了这种关系[46]。值得注意的是,尽管铜(II)和锌(II)的阳离子半径相似,但锌(II)的亚氨基二乙酸配合物与2,2′-联吡啶的取代反应的kobs值却高出约13倍。
图8
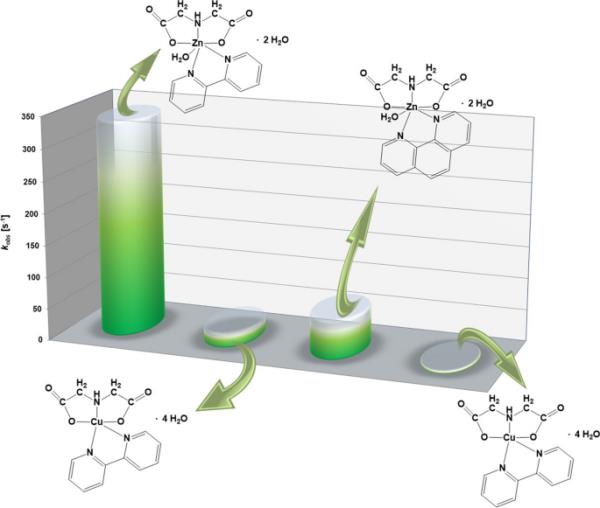
298.15 K时,过渡金属阳离子(1 mM)与苯环或苯(0.05 mM)在CTAB水溶液中亚氨基二乙酸配合物的可观测速率常数kobs [46]
图9
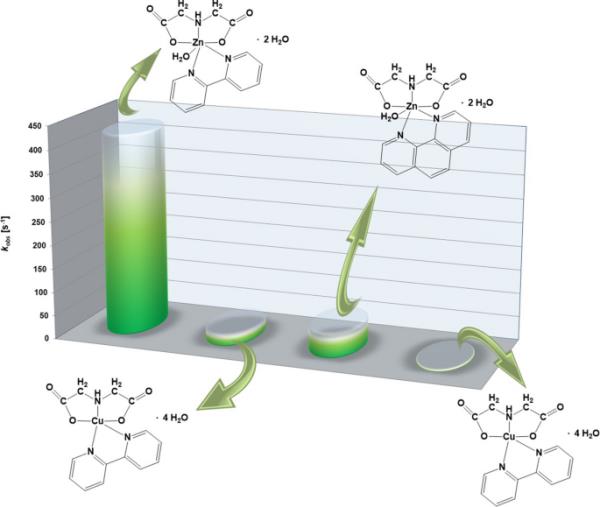
298.15 K时Triton X-100水溶液中过渡金属阳离子(1 mM)与双酚或苯(0.05 mM)的亚氨基二乙酸配合物的可观测速率常数kobs [46]
本文报道了表面活性化合物(CTAB和Triton X-100)对两个水分子被1,10-菲罗啉或2,2′-联吡啶取代反应动力学的影响。用停流分光光度法测定了反应动力学。根据在一定温度下[Zn(IDA)(H2O)2]配合物浓度对可观察速率常数的依赖性,可以得出随着配合物温度和浓度的升高,可观察速率常数kobs的值增大。这种依赖性与活性配合物的理论是一致的。根据配体取代的动力学研究,与2,2′-联吡啶的反应比与1,10-菲罗啉的反应更快。这可能是由于配体分子的大小——bipy比phen分子量小,而且bipy的碱性比phen弱。比较配体的性质,亚氨基二乙酸酯具有弱碱性,因为它的结构中有一个给体氮原子,因此在碱性较弱的bipy的情况下,取代反应进行得更快。
下载原文档:https://link.springer.com/content/pdf/10.1007/s11144-023-02453-5.pdf




