本研究旨在通过多尺度熵(MSE)、脑电信号标准差(SDs)、绝对谱功率(PSD)的均值、标准差(SDp)和变异系数(CV)分析脑电信号的复杂性和变异性,探讨ADHD与健康儿童的神经机制。为此,根据试验数和诊断一致性,选取6 - 17岁的ADHD患儿为样本,其中32例为睁眼(OE)实验,25例为闭眼(CE)实验。健康对照组与ADHD组的年龄和性别相匹配。采用粗粒度方法计算静息状态脑电活动在34个时间尺度上的MSE和sd。在delta、theta、alpha和beta频段平均PSD,并计算其平均值、SDp和CV。结果表明,在发育过程中,MSE随年龄变化,随量表数量的增加而增加,对照组的幅度高于ADHD组。绝对PSD结果显示受试者之间在低频段和β频段的CV差异,ADHD组的变异性值更高。所有这些结果表明,与对照组相比,ADHD患者脑电图变异性增加,复杂性降低。
儿童时期常见的神经发育障碍之一是注意缺陷多动障碍(ADHD)。其主要症状包括注意力缺陷、多动和/或冲动。这种障碍影响儿童的正常发展、课程活动和表现,导致学习和社会问题的高风险(Magnin & Maurs 2017)。在这些儿童中观察到的神经心理差异可以通过两种神经认知模型来解释:成熟延迟模型和差异发展模型。成熟延迟模型表明,ADHD儿童与正常儿童相比,发育时间较长(即ADHD儿童的脑电图和行为参数均呈现较年幼对照儿童的特征;Kinsbourne 1973;Matsuura et al. 1993)。差异发育模型表明,由于遗传或传记背景,ADHD受试者与对照组相比,在发育轨迹上观察到不同的参数模式(Giertuga et al. 2017;Saad et al. 2018;Rodríguez-Martínez et al. 2020)。
几项研究分析了ADHD的神经相关性,特别是与通过脑电图定量测量大脑信号相关的研究(Newson & Thiagarajan 2019;Clarke et al. 2020)。这些主要基于线性测量,例如涉及谱功率分析的测量,它显示了静息状态条件下(Clarke et al. 2020)和认知信息处理期间(Nazari et al. 2011)的非典型神经元模式。在快频段(β)频谱功率降低,在慢频段(δ和θ)频谱功率增加;Barry et al. 2009;Newson & Thiagarajan 2019;Clarke et al. 2020;Rodríguez-Martínez et al. 2020)。此外,据报道,θ / β比值(TBR)和θ / α可能是ADHD的鉴别标志(Barry et al. 2003, 2009)。然而,结果是高度可变的。例如,Giertuga等人(2017)显示,与对照组相比,ADHD的所有频带都有所减少。使用TBR进行诊断仍存在不确定性(Arns等人,2013;Saad et al. 2018)导致需要精确的测量方法,以便更准确地表征ADHD与对照组相比的神经生理差异。
在过去的几十年里,EEG信号的非线性分析,如底层神经网络的可变性和动态复杂性已经实现(Takahashi et al. 2009, 2013;garrett et al. 2013;Van Noordt & Willoughby 2021)。这些都是基于人类大脑是一个复杂的非线性系统,其复杂的时空波动是其内在活动的一部分(Takahashi et al. 2009)。从这个意义上说,非线性分析可以发现细微的变化,从而找到解释复杂神经动力学的新方法(Pincus 2006;Sohn et al. 2010)。可变性提供了对神经信号值范围的估计,可以通过不同的度量来测量,例如标准差(Garret et al. 2013)或变异系数(CV) (anglo - ruiz, et al. 2021)。另一方面,复杂性量化了这些信号中包含的信息,并检查了一个或多个时间尺度上的不规则性或可预测性(garrett et al. 2013)。因此,它决定了在时间序列中发现特定或相似模式重复的概率(Costa et al. 2002, 2005)。它是通过诸如熵(Kolmogorov 1958;Pincus 1991,1995;Richman & Moorman 2000;Takahashi 2013),或多尺度熵(MSE) (Costa et al. 2002, 2005;高桥2013)。MSE意味着内在的生理复杂性,允许区分噪声和有意义的复杂性,并检测长期的时间相关性,这是由于跨多个时间尺度的分析(Costa等人,2002,2005;Takahashi et al. 2009)。因此,MSE可以,首先,反映神经生理动力学,其次,表明非典型模式暗示大脑疾病状况(Costa等人,2002;Mizuno et al. 2010)。Bosl等人(2022)最近的一项研究发现,粗粒化过程中测量的尺度(从细到粗)与功率谱密度(PSD)的频带有关,这两个指标之间建立了直接关系。
与这些测量相关的研究指出,在开发过程中,变异性和复杂性会增加(McIntosh et al. 2008;Lippe et al. 2009;garrett et al. 2013;Szostakiwskyj et al. 2017;Van Noorddt & Willoughby 2021;anglo - ruiz et al. 2021),随着正常衰老而减少(Takahashi et al. 2009;Nomi et al. 2017)。然而,就变异性而言,可能的区域特异性(Nomi et al. 2017)和振荡频率(anglo - ruiz et al. 2021)必须作为影响脑电图成熟研究的潜在因素加以考虑。此外,在成熟过程中,复杂性在前中部区域表现出更显著的增加和变化(Van Noordt & Willoughby 2021)。Szostakiwskyj等人(2017)发现,细鳞的MSE随着年龄的增长而增加,粗鳞的MSE则下降。这些术语是MSE计算的时间尺度范围的标识符。因此,细尺度对应于对少量信号点(单个时间样本)进行平均的情况,粗尺度对应于对许多信号点进行平均的情况。值得注意的是,目前还没有标准范围来区分这些量表(Shen et al. 2021)。
复杂性已在不同临床人群中进行过研究(Takahashi et al. 2010;Fernández et al. 2013;Li et al. 2018)和神经发育障碍(Catarino et al. 2011;Bosl et al. 2011, 2017;Chu et al. 2017)。ADHD的结果仍然很少,不一致和异质性,显示出不同甚至相互矛盾的结果(Fernández et al. 2009;Sohn et al. 2010;Gómez et al. 2013;Sokunbi et al. 2013;Li et al. 2016;Rezaeezadeh et al. 2020;Hu et al. 2021)。具体而言,在脑电图中,ADHD儿童的复杂性增加(Li et al. 2016)和复杂性降低(Rezaeezadeh et al. 2020)。表1显示了ADHD和对照组在复杂性指标上的差异。一般来说,脑电图异常复杂性与脑部疾病是一致的(Takahashi 2013;Chu et al. 2017)。因此,复杂性的增加或减少可能导致信息处理效率低下(Ghosh et al. 2008;McIntosh et al. 2008,2010),异常的潜在生理动力学(Takahashi 2013)和异常的神经元连接(Takahashi et al. 2016)。因此,有人认为健康的大脑更加可变和复杂(Garrett et al. 2013),异常的可变性和/或复杂性水平可能与次优认知有关(Nomi et al. 2018;Easson & McIntosh 2019)。
表1 ADHD及co的复杂性文献综述控制组织
全尺寸工作台
我们建议使用MSE分析脑电图的脑信号复杂性,以探索ADHD儿童与健康儿童样本的潜在神经机制。考虑到MSE是表征脑疾病非线性异常的敏感指标,MSE是在睁眼(OE)和闭眼(CE)实验条件下计算的(Chu et al. 2017;Shen et al. 2021)。然而,目前还没有这样的申请被批准用于临床。此外,还计算了SDs EEG(不同尺度EEG的标准差)、不同脑节律下的绝对PSD(平均值、试验间标准差(SDp)、试验间变异系数(CV))和相对PSD的平均值,作为补充测量,提出了综合表征对照组和ADHD的方法。目前的研究假设(i)与正常发育的儿童相比,ADHD儿童将表现出复杂的非典型神经模式。此外,尽管大多数研究表明,在分析的所有尺度上,MSE随着年龄的增长而增加,但Szostakiwskyj等人(2017)已经显示出MSE与年龄之间关系的正斜率和负斜率,这取决于尺度,因此我们打算在两组中测试这些斜率的稳定性或可变性。(ii)对于SDs,我们预计两组中所有量表的脑电图变异性随年龄下降,脑电图振幅随年龄下降。两组之间的比较将表明脑电图变异性是否也可能是区分ADHD与对照组的合适指标;(iii)对于绝对PSD和SDp,我们预计在不同脑节律(CV)的PSD均值归一化时,低频段的组间幅度差异以及随年龄的变异性差异会随着年龄的增长而减少;(iv)相对PSD的低频段与年龄呈反比关系,而在高频段呈正相关,考虑到在MSE中,更高的尺度代表越来越低的频段。所有尺度都包含最低频率(Bosl et al. 2022)。该方法旨在提供基于脑电图变异性、复杂性和能力的神经生理指标在对照组和ADHD受试者中的区别,以解释该疾病可能的神经原因,进而找到有助于诊断的生物标记物。
一组由两家公立医院的临床专家诊断为多动症的儿童和青少年参与了这项研究。采用结构化访谈和DuPaul家长问卷(DuPaul et al. 1998)进行诊断。ADHD组由40名6 - 17岁的儿童和青少年组成,在实验性OE和CE条件下进行记录。只有(i)在一种或两种情况下(OE和CE)获得至少50次试验且无伪像的受试者,以及(ii)在问卷调查和临床诊断之间显示诊断一致性的受试者才被选中进行数据分析。因此,ADHD组最终由32例OE组儿童青少年(M=10.94, SD=3.18,男性25例,女性7例,6-17岁)和25例CE组儿童青少年(M=11.8, SD=3,男性21例,女性4例,7 - 17岁)组成。由于每组受试者人数较少,未按ADHD类型进行分组。
采用可及性抽样的方法,从公立学校选取年龄、性别与ADHD实验条件相匹配的OE对照组(M=10.84, SD=3.10,男25人,女7人,6-17岁)和CE对照组(M=11.68, SD=2.93,男21人,女4人,7 - 17岁)32人。CE的对照受试者减少到25人,使其与CE条件下的ADHD受试者数量相等。两组患者年龄差异无统计学意义(OE: F (1,62)=0.000042, p=0.995;eta偏平方=0.0000007)和CE:(F (1,48)=0.000122, p=0.991, eta偏平方=0.000003)或性别(OE: (F (1,62)=0.00, p=1;eta偏平方=0.00)和CE:(F (1,48)=0.00, p=0.991, eta偏平方=0.00)。性别和年龄在控制组和ADHD之间的相等使得这些因素在平均比较统计分析中得以消除。
对照组没有报告神经系统疾病、癫痫发作症状或心理障碍。实验方案经Andalucía自治区生物医学研究伦理委员会批准。遵循了《赫尔辛基宣言》的指导方针,并获得了家长的书面知情同意。
在OE和CE实验条件下获得自发性脑电图活动,持续时间为3分钟。受试者被指示在两种实验条件下保持静止并保持放松状态。在OE条件下,他们还被要求尽可能少地眨眼,并看着屏幕中央的一个十字架。
使用按照国际10-20体系组装的32电极帽(ELECTROCAP) (Fp1、Fpz、Fp2、F7、F3、Fz、F4、F8、FC5、FC1、FC2、FC6、M1、T7、C3、Cz、C4、T8、M2、CP5、CP1、CP2、CP6、P7、P3、Pz、P4、P8、POz、O1、Oz、O2)进行记录。放置在头皮上的电极离线参考平均乳突(M1 + M2)/2。在每只眼睛的外缘放置两个电极来记录水平的眼球运动,在左眼的上下放置两个电极来记录垂直的眼球运动。阻抗在10科姆以下。使用模拟-数字采集和分析系统(ANT放大器,荷兰),在512 Hz直流电下以20,000增益记录数据,没有任何滤波。
EEG数据分析使用EEGLAB工具箱(Delorme & Makeig 2004)和Matlab R2019a软件包。
对EEG信号进行0.5 ~ 35 Hz的带通滤波(eegfilter -新的EEGLAB功能)。采用伪影子空间重构(ASR)算法对校准数据(干净原始数据EEGLAB函数)标准差超过20倍的脑电信号伪影进行校正。重建数据,拒绝任何通道中超过±120 μV的epoch(持续时间2 s)进行后续分析(EEGLAB功能)。少于50次试验的受试者没有进一步分析。表2显示了各组接受的epoch数和实验条件。方差分析比较显示,两组患者接受的epoch数没有差异:OE组(F (1,62)=0.147, p=0.703, eta偏方=0.002)和CE组(F (1,48)=1.3, p=0.259, eta偏方=0.026)。
表2在睁眼(OE)和闭眼(CE)条件下,对照组和ADHD受试者接受试验的均值和标准差
在Costa等人(2005)的基础上,使用Matlab (Malik 2022)的“multiscaleSampleEntropy”函数计算所有通道(M1和M2除外)的MSE。MSE分析是Shannon熵(Shannon & Weaver 1949)和Pincus近似熵(Pincus 1991)的派生。它是基于多个时间尺度下脑电信号的采样熵(SampEn)的计算(Costa et al. 2002,2005;Richman & Moorman 2000)。MSE是信号复杂性的指标(Garrett et al. 2013),并使用称为粗粒度的过程计算。每个时间尺度通过平均原始时间序列(长度为τ)的不同相邻点来定义,将不同数量样本的非重叠窗口中的脑电信号分开。然后,计算每个时间尺度的SampEn。该分析评估了m个数据点(p^m)与m + 1个数据点(p^(m + 1))的模式重复频率的相似性。为此,有必要定义一个相似性限制(r),该限制限定了被认为相似的单个数据点的容忍范围(k)。相似性限制通过EEG标准偏差(SD) k < r × SD进行归一化(Malik 2022)。
最近,有人提出粗粒度过程可与Haar小波近似在2次幂尺度上相媲美,将传统频谱功率分析的不同频段与MSE的不同尺度联系起来(Bosl et al. 2022)。从这个意义上说,较粗的尺度将包含经过高频滤波的较低频率(Kosciessa et al. 2020),较低的尺度是具有高频的原始信号,所有尺度也包含低频(Bosl et al. 2022)。
在我们的研究中,我们将参数m=2和r=0.5考虑到以前的EEG信号复杂性研究给出的建议(Richman & Moorman 2000;McIntosh et al. 2008;Miskovic et al. 2016;Kosciessa et al. 2020;Kloosterman et al. 2019),其中SD参数允许通过每个特定尺度的EEG标准差对r参数进行归一化。计算时间尺度为1 ~ 34的MSE,可以分析从最细到最粗的熵,也可以间接分析低频段(≤7.73 Hz)的熵。最后一个时间尺度对应于每个时间点64.6 ms,每次试验31个时间点。
用于计算SampEn的方程为(Malik 2022),采用Kosciessa et al.(2020)的符号:
SampEn的高值表明存在低时间规律性或高复杂性(即许多长度为m的模式在长度为m + 1时不会重复),而低值表明高相似性/规律性或低复杂性,表明信息匮乏(McIntosh et al. 2008;Garrett et al. 2013)。
两组和两组的EEG标准差(SDs)采用与MSE相同的量表计算。计算各试验的脑电图变异数(EEG SDs),得到各试验在不同尺度下的SDs均值。该参数可以告知两组在不同量表和不同年龄时脑电图的变异性是否不同(通过将SDs与年龄相关)。SDs参数提供了EEG的基础变异性,可以与提供每个EEG频率能量的PSD和提供数据复杂性的MSE相补充。
计算每个受试者在两种实验条件下(OE和CE)的绝对PSD的平均值。PSD在2 s窗(1024个采样点,采样率为512 Hz)内计算,使用EEGLAB频谱函数,该函数采用Matlab pwelch函数应用hamming窗。spectopo计算绝对PSD的对数(Y=10 * Log (PSD)),通过去除对数(PSD=eY/10)来计算每个受试者的PSD值(跨试验的PSD均值(M)和标准差(SDp)),以可视化数据并计算跨试验的变异系数(CV)。在随后的分析中,考虑了四个不同范围内的平均频段:delta (1-2 Hz)、theta (4-7 Hz)、alpha (8-11 Hz)和beta (13-20 Hz)。由于在数据分析中使用了带通滤波器(0.5-35 Hz),以消除高频肌电伪影,因此没有计算伽马带。
相对PSD的计算采用每个受试者在每个电极处的绝对PSD的平均值(去除对数),计算公式如下:
其中X(fi)是给定频率的相对PSD, PSD (fi)是给定频率的绝对PSD,是所有考虑频率(1-20 Hz)的绝对PSD之和。该分析在两种实验条件下(OE和CE)对对照组和ADHD进行。
为了计算各组之间的MSE、sd、绝对PSD(平均值和CV)和相对PSD指标的平均值的差异,将图1中定义的相邻电极上的这些参数值折叠,以降低OE和CE的数据维数(图1)。为了同样的目的,34个时间尺度的MSE结果被组织成三个更大的尺度(以ms为单位的值对应于尺度时间采样):精细尺度(1.9 ms(尺度1)-24.7 ms(尺度13));中刻度(26.6 ms(刻度14)-43.7 ms(刻度23));Szostakiwskyj等人(2017)提出的粗尺度(45.6 ms (scale 24) -64.6 ms (scale 34))。通过将EEG样本周期乘以量表的顺序来计算量表的周期。
图1
电极的区域定位和塌陷。这些颜色表示电极崩溃的九个确定的头皮区域。30个电极被分为两个空间维度(横向和前后),每个维度有三个值:左、中、右;分别是前部,中央和后部
采用社会科学统计软件包25 (SPSS)对如上所述和图1中定义的每个脑区域的每种类型的量表(细、中、粗)的MSE的平均值进行了三次方差分析(ANOVA)。对于第一次和第二次方差分析,受试者内因素为:量表类型(水平:细、中、粗)、前后区域(水平:前、中、后)和外侧区域(水平:左、中、右);受试者间因素为组(对照组和ADHD受试者)。前两个方差分析分别对应于OE和CE条件的独立分析。在第三个方差分析中,我们加入了实验条件(OE和CE)作为受试者内因素,保持了之前考虑的因素。对于具有OE和CE两种情况的相同受试者,第三次方差分析分别只剩下23名对照和25名ADHD。当在方差分析中发现显著的组差异时,独立样本t检验(错误发现率(FDR)修正)作为事后检验计算(Benjamini & Hochberg 1995)。对于所有考虑的因素,方差分析的统计结果都具有统计学意义,但考虑到本报告的主要目的是组间差异,只有那些包括群体因素的因素在事后检验中进行了讨论和分析。
此外,在两种实验条件下(OE和CE),分别对对照组和ADHD进行独立的MSE与受试者年龄(以天表示)的Spearman相关性分析。为了进行相关分析,我们将所有电极上的MSE值折叠以降低维数。在计算相关分析的其他变量中,电极的崩溃也被应用。
34个量表的脑电SDs经电极折叠后,采用与MSE相同的统计分析程序。(i)与年龄的Spearman相关性,(ii)有和没有因素“实验条件”(OE和CE)的三种方差分析(ANOVA),以及(iii)用于事后分析的独立样本t检验(FDR校正)。
对于绝对PSD统计分析,在每个考虑频率(1-20 Hz)的电极上平均PSD的崩溃与受试者的年龄(以天表示)之间进行Spearman相关性。对SDp、CV和相对PSD进行了相同的相关分析。此外,对于相对PSD,我们将不同频率下各组相对PSD与不同MSE尺度与实验条件进行相关性分析。变异系数由绝对PSD (SDp)的标准差除以所有受试者、两种实验条件(OE和CE)和每个频率(1-20 Hz)的绝对PSD (CV=SDp/M)的平均值计算。通过三个方差分析分析绝对PSD和相对PSD和CV的均值。第一个(OE条件)和第二个(CE条件)方差分析包括受试者内因素:正面区域和侧面区域,以及组间因素。第三个方差分析增加了受试者内因素“实验条件”(OE vs CE)。方差分析对四个不同的考虑频带(delta, theta, alpha和beta)进行独立计算。
FDR是根据Benjamini & Hochberg(1995)计算的,用于事后分析和相关分析,作为多重比较和Spearman相关性的控制措施。
摘要
介绍
方法
结果
讨论
结论
参考文献
致谢
作者信息
补充信息
搜索
导航
#####
图2和图3分别显示了OE和CE实验条件下的MSE结果。MSE随着尺度数量的增加而增加。虽然数据表明ADHD组在OE和CE方面的MSE值低于对照组,但方差分析(表3)显示,对照组和ADHD组(MSE对照组> MSE ADHD组)之间的统计学显著差异仅存在于OE条件下。如方法部分所示,对有足够试验数的受试者进行方差分析,将实验条件(OE & CE)作为组内因素(表4)。后一方差分析显示对照组和ADHD组之间存在统计学显著差异。
图2
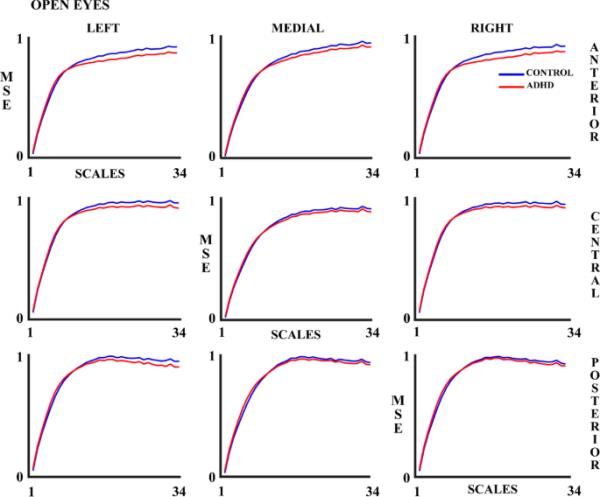
对照组和ADHD被试在睁眼(OE)实验条件下的34个量表的多尺度熵(MSE)。蓝线代表对照组,红线代表多动症组
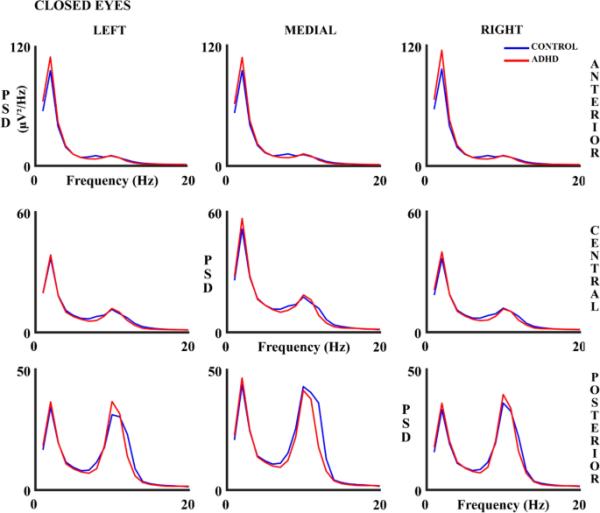
图3
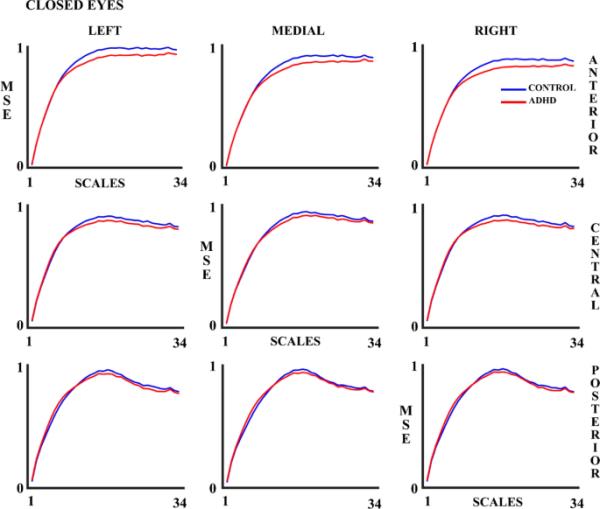
对照组和ADHD被试在闭眼(CE)实验条件下的34个量表的多尺度熵(MSE)。蓝线代表对照组,红线代表多动症组
表3多尺度熵值方差分析的显著性结果,与因素组被试(co对照和ADHD),鳞片(细,中,粗),侧边和前后,独立用于睁眼(OE)和闭眼(CE)条件
表4显著性多尺度熵值方差分析结果,与因素组被试(co .控制和ADHD),鳞片(细,中,粗),侧边,前后,睁眼和闭眼条件(OE & CE)
尽管Spearman相关性(表5和表6)在精细尺度上显示MSE与受试者年龄(以天为单位)呈正相关,但在较粗的尺度上,这种关系相反,对于实验条件(OE和CE)和两组(对照组和ADHD)都是如此。在CE条件下,对照组(M=0.521, SD=0.172)与ADHD受试者(M=0.356, SD=0.156)(基于绝对相关值之间的t检验)的相关性(绝对值)更大(p < 0.001)。
表5不同尺度MSE与年龄(以天表示)的Spearman相关性(Rho)对照组和ADHD组在睁眼(OE)条件下
表6不同尺度MSE与年龄(以天表示)的Spearman相关性(Rho)对照组与ADHD组闭眼观察ndition (CE)
在两种实验条件下,脑电图变异性(以SDs测量)显示随着量表数量的增加而减少(图4和5),对照组和ADHD儿童的脑电图变异性随年龄的增加而减少(补充表1和2)。
图4
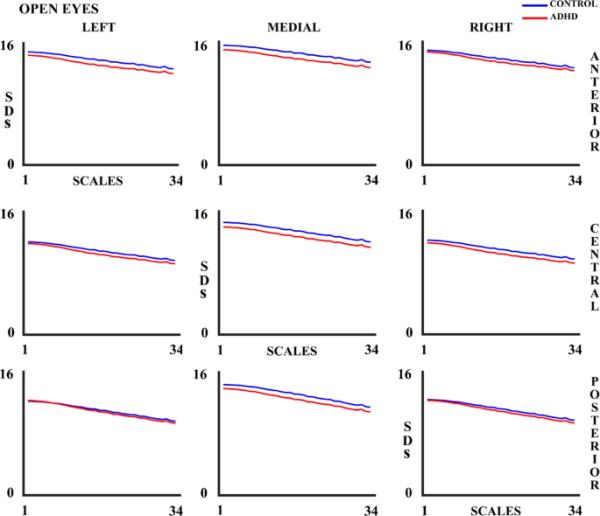
对照组和ADHD受试者在睁眼(OE)实验条件下34种量表在所有9个考虑区域的标准差(sd)。蓝线代表对照组,红线代表多动症组
图5
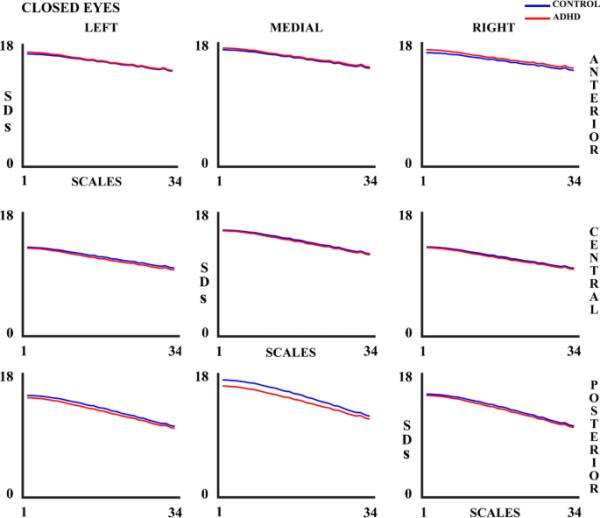
对照组和ADHD被试在闭眼(CE)实验条件下34种量表在所有9个考虑区域的标准差(sd)。蓝线代表对照组,红线代表多动症组
在受试者内因素之间没有观察到主要或交互作用。OE、CE和CE&OE的所有受试者内显著性方差分析结果显示在补充表3和4中,但未进一步分析。
图6和7显示了两种实验条件下所有分析的头皮区域的绝对PSD结果。这些数据表明ADHD儿童的PSD在δ (CE)和α频带(OE)中较高,主要在前部和后部区域。然而,方差分析结果(补充表5)显示,单独对OE和CE而言,x侧x前后相互作用组的α频带有显著影响。方差分析显示,因素组x侧后侧面积对OE的影响(F (1.83, 113.7)=3.41, p=0.040;偏平方=0.052)。这种相互作用是由于与ADHD相比,对照组左后侧区域和中后侧区域的α PSD差异更大(p=0.023)。然而,在CE的事后方差分析中,在任何选定的区域都没有与组的相互作用。
图6
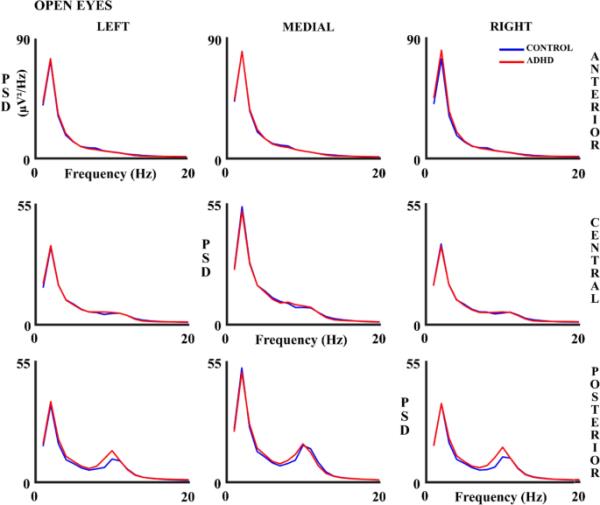
以Hz为单位的绝对功率谱密度(PSD)在对照组和ADHD受试者睁眼(OE)实验条件下的所有9个考虑区域。蓝线代表对照组,红线代表多动症组
图7

绝对功率谱密度(PSD)在对照组和ADHD被试闭眼(CE)实验条件下的所有9个考虑区域。蓝线代表对照组,红线代表多动症组
包括实验条件(OE & CE)作为受试者内因素的绝对PSD分析结果(补充表6)显示了delta波段中组与实验条件之间的相互作用。事后分析(F (1,46)=5.39, p=0.025;偏方=0.105)显示ADHD患儿CE与OE的绝对PSD值差异较大(M=1.55;SD=1.17),与对照组相比(M=0.834;sd=0.936)。
两种实验条件下的Spearman相关结果均显示,各频段PSD的均值(补充表7和8)和标准差与年龄(补充表9和10)呈负相关。
补充表11显示了OE和CE条件下CV的方差分析结果。在两种实验条件下,对照组和ADHD组在delta波段的CV上都有显著差异。在OE CV值中,ADHD组(M=1.8, SD=0.069)高于对照组(M=1.77, SD=0.067), CE组(ADHD组(M=1.83, SD=0.083)和对照组(M=1.77, SD=0.065)。包括群体因素在内的相互作用的影响在OE的θ和β波段上显示出正相关差异。然而,在进行多重比较分析时,只有β带的前部区域在两组之间存在差异(p=0.01): ADHD组的CV值较高(M=1.69;SD=0.083),与对照组(M=1.64;sd=0.043)。
将实验条件(OE&CE)作为受试者内因素(补充表12)的CV分析结果显示,由于ADHD的CV幅值较高(M=1.82, SD=0.055),组与对照组(M=1.77, SD=0.054)在δ波段上存在差异。波段显示了组和实验条件之间的相互作用。即ADHD组(p=0.012) OE的CV值较高(M=1.67;SD=0.050),与CE相比(M=1.64;SD=0.028),而对照组两组间无差异。组与theta波段的前后区之间的相互作用表明,在对照组中,区域之间的比较是显著的:前区CV值为前区CV值(p < 0.001)、前区CV值为后区CV值(p=0.008)、中区CV值为后区CV值(p=0.018) (M=1.69;SD=0.052)和后区(M=1.65;SD=0.055)高于中央(M=1.63;sd=0.039)。在ADHD组中,区域间的比较只有前中央区(p < 0.001)和前后区(p < 0.001),其中前区(M=1.71;SD=0.079), CV值高于后区(M=1.63;SD=0.021),中心区域(M=1.62, SD=0.023)。β带组OE&CE x前后相互作用在对照组之间存在差异(M=1.64;SD=0.036)和ADHD (M=1.7;SD=0.088),在OE情况下的前区(p=0.005)。当进行多重比较修正(FDR)时,ANOVA中其他重要的相互作用失去了其显著性。CV与年龄的相关性在任何组或情况下均不显著。
相对PSD分析的结果(表7)显示了OE条件下alpha波段侧x前后x组区域之间的相互作用。事后分析显示,不同地区或群体之间没有差异。包括条件、OE和CE(表8)在内的分析,作为受试者内因素,显示了delta波段组间的差异。这一差异是由于对照组OE和CE的相对PSD值(M=2.57, SD=2.88)高于ADHD组(M=0.53, SD=3.01)。
表7相对PSD的方差分析结果与以下因素有关:受试者组、前后位和侧位
表8显著性方差分析结果的相对PSD值,与因素组受试者(co对照和ADHD),侧边,前后眼,睁眼和闭眼条件(OE和CE),每个波段独立
实验条件OE(表9)和CE(表10)的Spearman相关结果表明,随着年龄的增长,相对PSD在慢频段降低,在快频段增加。在CE条件下,对照组(M=0.435, SD=0.181)与ADHD受试者(M=0.325, SD=0.118) (p=0.029)(基于绝对相关值之间的t检验)有更大的相关性(绝对值)。
表9相对PSD与年龄(天)的Spearman相关性对照组与ADHD组的比较ndition (OE)
表10 co .的相对PSD与年龄(单位:天)Spearman相关性对照组与ADHD组闭眼观察ndition (CE)
相对PSD (1-20 Hz)与量表(34个量表)(图8A)之间的相关性结果显示,OE(对照组)(Rho截止值> 0.39,p < 0.025)、ADHD (Rho截止值> 0.39,p < 0.027)、CE(对照组)(Rho截止值> 0.47,p < 0.017)、ADHD (Rho截止值> 0.45,p < 0.022)之间存在显著的正相关(经FDR校正),OE和CE条件下均存在显著的负相关。高频(beta)和精细量表(1-13量表)和低频(delta, theta)与粗量表(24-34量表)之间存在显著的正相关,而高频与粗量表和低频与中量表(14-23量表)之间存在显著的负相关。这些结果支持两个指标之间的关系。计算偏相关以控制受试者年龄的影响,MSE与相对PSD之间存在显著相关。与不受年龄控制的相关性(图8A)相比,在控制年龄的相关性中观察到类似的模式(图8B),这表明在两组和条件下,成熟度对这些指标的影响都很低。
图8
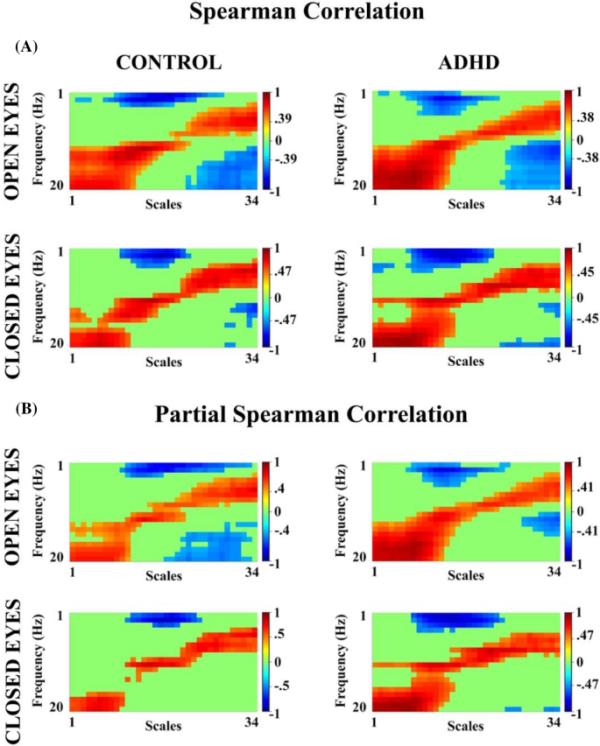
在两种实验条件下,对照组和ADHD被试的MSE(34个量表)与相对PSD (1-20 Hz)之间的Spearman相关性B部分Spearman相关性,控制两组被试在睁眼和闭眼条件下的年龄(以天为单位)。每个相关性的截止值,经FDR校正后是显著的,在图中表示。红色表示正相关,蓝色表示负相关
最后,在ADHD (OE和CE)组中,计算了所分析的不同测量值之间的Spearman相关性:MSE、sd、绝对PSD(平均值和CV)和相对PSD与DuPaul问卷中冲动和注意力不集中的行为测量(DuPaul et al. 1998)。没有发现显著的结果。
在OE和CE的实验条件下,我们使用MSE、sd和PSD(绝对(平均值、SDp和CV)和相对(平均值))方法分析了一组ADHD儿童与年龄和性别匹配的规范组的对比,观察了脑节律可能的改变,并评估了神经脑电图的复杂性和可变性。我们假设,与ADHD儿童相比,对照组儿童在EEG MSE和变异性方面存在差异,并且所有EEG指标与年龄之间存在很强的相关性。
对于不同EEG指标与年龄的相关性分析,许多研究支持内源性皮层动态复杂性随年龄在较低频段的增加(McIntosh et al. 2008, 2010;Garrett et al. 2013;Miskovic et al. 2016;Van Noordt & Willoughby 2021)。这种增长可能是网络功能重新配置的结果,随着年龄的增长,网络功能从更稳定的状态转变为更可变的状态。脑成熟过程中的脑网络功能组织与MSE有关(McIntosh et al. 2008, 2010)。然而,我们的研究表明,在OE和CE条件下,年龄在不同尺度上的正相关关系是有限的。结果表明,在静息状态下评估的34个时间尺度中,MSE与年龄之间的关系呈倒转关系(由正向负)。MSE与年龄之间的关系由正向负的倒转在两组中都出现了:对照组和ADHD组。这与Szostakiwskyj等人(2017)发现的结果一致,他们认为随着尺度数量的增加,MSE随年龄的增加逐渐减弱,在粗时间尺度上达到相反的关系。因此,Szostakiwskyj等人(2017)的研究和我们的研究都支持这样一种观点,即在两组(对照组和ADHD)中,随着年龄的增长,整个大脑的局部信息处理都会增加(在精细尺度上,mse -年龄呈正相关),并且,在发育的后期,由于低频在粗尺度上占主导地位,远程神经群体之间的相互作用会减少(在中、粗尺度上,mse -年龄呈负相关)(Szostakiwskyj等人,2017)。
同样,先前关于PSD的研究表明,随着年龄的增长,高频波段的增加(Segalowitz等人,2010)与局部信息的处理增加有关;而低频率的减少对应于与其他神经元群的远程交流的减少(Gasser等人,1988;Von Stein et al. 2000;McIntosh et al. 2008;Cragg et al. 2011)。MSE研究表明,尺度包含频率信息,细尺度包含所有频率信息,粗尺度包含低频信息(McIntosh et al. 2008, 2010;Szostakiwskyj et al. 2017;Bosl et al. 2022)。我们的研究结果支持这些陈述,表明相对PSD和MSE与年龄之间存在很强的关系,表现为高频频段和细尺度的增加,以及低频频段和粗尺度的减少,间接涉及连通性细化模式。同样,在开发过程中,以聚类系数和路径长度随年龄增长而增加为特征的小世界拓扑的建立(Boersma et al. 2011)与MSE和相对PSD的增减之间可能存在间接关系。正常发育人群的脑电图研究表明,随着年龄的增长,聚类和路径长度系数增加,小世界拓扑结构在发育过程中有所增加(Boersma et al. 2011;Smit et al. 2012;vsamrtes & Bullmore 2015)。振荡频率也与大脑的连通性有关;因此,低频反映大脑的整体活动,高频反映其局部连通性(Li et al. 2016)。目前的研究结果显示,与ADHD相比,对照组的MSE(从细到粗,从高频到低频)和相对PSD(从低频到高频)随年龄的反转模式更一致,这表明在神经网络中,随着成熟,局部分离和远程精细集成拓扑结构在对照组中比在ADHD中更明显地建立起来。
调查整个发育过程中平均PSD的研究表明,所有脑节律的绝对功率普遍下降,低频频段减少,高节奏相对功率增加(Dustman等,1999;McIntosh et al. 2008;Barry et al. 2009;Segalowitz et al. 2010;Rodríguez-Martínez等人,2012,2017,2020)。本研究的结果证实,在两组分析中,绝对PSD与年龄以及OE和CE呈负相关,验证了这一EEG参数是EEG成熟的可靠生物标志物(Gasser et al. 1988;Segalowitz et al. 2010;Rodríguez-Martínez et al. 2012;Miskovic et al. 2015)。从这个意义上说,PSD随着年龄的增长而下降可以用突触修剪的过程来解释,在这个过程中,最稳定的神经连接被维持,其余的被修剪,增加了神经传递的效率(Whitford et al. 2007)。年龄与相对PSD相关性的反转,从低频的负相关到正相关,决定了随着成熟的进展,高频对脑电图功率的贡献更高(Segalowitz et al. 2010)。另一方面,两组间PSD(绝对和相对)的主要差异出现在δ和α频段。对于delta波段,ADHD组绝对PSD的条件差值(CE-OE)高于相对PSD,相对PSD的这些值高于对照组。在α波段上,OE组的绝对PSD和相对PSD存在差异。然而,与ADHD相比,只有对照组的绝对PSD在左后区和后内侧区之间表现出更高的差异值。虽然本报告没有发现ADHD的平均PSD在低频波段相对于对照组有所增加,但由于群体因素与实验条件的相互作用,我们获得了差异。后者可以通过相对较低的被试样本和ADHD儿童PSD的变异性来解释。同样,据报道,60%的受试者theta值升高,40%的受试者theta值降低(Clarke et al. 2011)。
上述相对PSD和MSE之间的高相关性,即使部分相关性受年龄控制,也表明这两个指标之间存在功能依赖关系,正如Bosl等人(2022)所建议的那样。同样,先前分析这种关系的研究发现,在低、中尺度(高频)的MSE和相对PSD之间的关系也存在类似的模式(McIntosh等人,2008;Kosciessa et al. 2020;Van Noord & Willoughby, 2021)。考虑到尺度和频带之间的这种关系(Bosl et al. 2022),以及本研究使用512 Hz的采样率和34个尺度(频率≤7.73 Hz的较高尺度),最粗的尺度相当于delta和theta波段,中等尺度相当于alpha和低beta,精细尺度相当于beta。重要的是要注意,由于高通滤波器的伽马波段或以上,它不被考虑。然而,MSE对EEG信号不规则性的线性和非线性时间依赖性敏感,而PSD仅对线性变化敏感(Van Noordt & Willoughby 2021)。本报告中未发现对照组与ADHD的相对PSD存在明显的直接差异(显著差异为因素效应的相互作用),而这些差异是在MSE中获得的,这是主要的群体因素效应,说明在ADHD和对照组的分析样本中,对照组与ADHD之间存在非线性的时间依赖性的成熟差异效应。
我们的脑信号跨尺度变异性(SDs)和频谱功率(SDp)的结果与MSE是互补的。全脑MSE随量表数量的增加(从高频段到低频段)和年龄的增加而增加和减少,SDs和SDp随年龄和两组(对照组- adhd)的两种实验条件的增加和频率(1-20 Hz)的减少。这些结果表明脑电图的变异性降低与脑电图绝对PSD随年龄的减少有关,在本研究结果中也观察到。随着年龄的增长,绝对频谱功率的下降伴随着EEG变异性的减少(SDs和SDp),这可能是神经修剪过程降低EEG振幅的结果(Whitford et al. 2007)。然而,SDs和SDp的计算与MSE的根本不同之处在于,MSE的计算考虑了试验的EEG标准差对相似极限(r)参数的归一化,在这方面,MSE的计算与CV在不同频带的试验中的变异性更相关,因为在CV中EEG的标准差是通过均值进行归一化的。无论是在对照组还是ADHD中,CV均未显示出年龄的调节,但各组间CV的平均比较显示,ADHD的δ和β节律CV与对照组相比有所增加,尤其是在前部区域。后者的结果表明,自发性脑电图在ADHD患者中比在对照组中更具有可变性。先前已经观察到ADHD受试者的行为和神经反应与对照组相比具有更高的可变性(Castellanos et al. 2009)。因此,目前的结果为ADHD受试者的激活水平与对照组相比有更多的变化提供了证据,而在ADHD对照组中获得了更高的复杂性。
由SDs、SDp和CV测量的EEG变异性可以被认为是变异性的一阶测量,它不能完全纳入不同时间尺度的有组织模式的存在。MSE结合了时间序列的可变性和组织性,因此非常适合分析生理信号(Garrett et al. 2013;McIntosh et al. 2010)。因此,对几种精神和心理障碍的复杂性分析显示脑电图异常(Catarino et al. 2011;Bosl et al. 2011, 2017;Chu et al. 2017;Takahashi et al. 2013;Papaioannou et al. 2021)。特别是在像多动症这样的发育障碍中,没有多少研究被进行,导致结果不一致。例如,Fernández等人(2009)发现ADHD组的复杂性(Lempel-Ziv复杂性(LZC))随着年龄的增长而下降,而对照组则有所增加;Rezaeezadeh等人(2020)使用MSE表明,ADHD儿童的复杂性值低于正常组;Li等人(2016)指出,与对照组相比,ADHD受试者的δ和θ节奏的复杂性值更高,α节奏的复杂性值更低。我们的研究结果表明,在两组分析中,对于OE和CE,复杂性在越来越粗的时间尺度上都有所增加。组间比较显示,与ADHD相比,对照组的MSE值更高,这表明在静息状态下,不同时间尺度(Szostakiwskyj et al. 2017)的神经信号越来越可变,越来越难以预测(Garrett et al. 2013)。最近,功能性近红外光谱(fNIRS)研究表明,ADHD儿童的初级和高阶功能性脑网络(如默认模式网络、额顶叶网络、注意力网络和视觉网络)的复杂性降低(Hu etal . 2021)。因此,在对照组中观察到的更高的复杂性可以反映出增加的信息处理能力(Szostakiwskyj et al. 2017),稳定的行为反应更加成熟(McIntosh et al. 2008;Misic et al. 2010),以及对环境不确定性的有效适应(Grady & Garrett 2018),强调了ADHD儿童在这些过程中的差异。因此,目前的结果表明,ADHD儿童比对照组表现出更多的脑节律变异性(如CV所示),但脑电图复杂性(如MSE所示)较低。
目前的结果支持成熟延迟模型,因为与对照组相比,ADHD受试者的复杂性降低,因为这些儿童的MSE值低于生物学年龄(Szostakiwskyj et al. 2017)。有趣的是,如前所述,ADHD表现出较不明确的模式(MSE与年龄的相关性较低),随着年龄的增长,精细量表的增加和粗糙量表的减少比对照组要少。类似的ADHD发展模式(相对PSD与年龄的相关性较低)也显示出相对PSD在低频时相对功率降低,而在高频时相对功率随年龄增加。后者的结果不仅表明了发育迟缓,而且表明了发育轨迹的差异,如组间MSE和相对PSD与年龄的相关性的显著差异。
与正常儿童相比,ADHD儿童脑电图的复杂性降低,变异性增加,以及PSD低频带的相互作用表明,与正常儿童相比,ADHD儿童在生理年龄的神经水平上表现出异常功能(Shaw et al. 2007;Narr et al. 2009;Giertuga et al. 2017;Saad et al. 2018;Rodríguez-Martínez et al. 2020)。然而,其他研究报告了复杂性和/或可变性的增加(Li et al. 2016),以及ADHD组OE中低频PSD的增加(Sohn et al. 2010;Nazari et al. 2011),因此仍需要进一步的研究来达成更一致的协议。一般来说,这些差异可能受到ADHD类型、药物管理和/或疾病合并症的变异性的影响。
因此,有必要提及本研究的局限性,例如分析的受试者数量,以及研究中纳入的女性人数较少。这可以解释为男性人群中这种疾病的患病率较高,在这个问题上,一些研究已经证明了ADHD患者的脑电图存在性别差异。与患有该疾病的男性相比,女性的脑电图更均匀,更少异常(Clarke et al. 2020),这可能会影响症状学,进而导致低水平的诊断。因此,在未来的研究中,建议将更多的妇女纳入研究。虽然建议最少50个样本才能可靠地估计MSE,而本报告仅使用31个样本进行最粗略的估计,但根据MSE与年龄相关性的模式反演结果,MSE的计算是准确的。然而,未来的研究将包括更长时间的静息状态记录,这将允许在更长的时期内分割EEG数据,并有足够的试验数量来计算更可靠的MSE估计。
目前的研究表明,与对照组相比,ADHD患者的MSE降低,脑电图变异性(CV)增加。这些结果表明,与对照组相比,ADHD患者的神经环境更不稳定,适应新情况的能力更低。结果还表明,在两组中,细鳞片的MSE随年龄增长而增加,而粗鳞片的MSE随年龄增长而减少。后者的结果表明,在发展过程中,局部连接得到加强,而远程连接得到完善,这与跨发展建立小世界网络拓扑是一致的,在对照组中比在ADHD中更均匀地建立起来。
以下是电子补充材料的链接。
下载原文档:https://link.springer.com/content/pdf/10.1007/s11571-022-09869-0.pdf




